2024(令和6)年度の薬価制度改革②補正加算について整理してみよう

参考記事:2024年度薬価制度改革の骨子(案)を承認、創薬力を評価医療機関が「後発品を安定供給できる企業」選ぶ指標を可視化
厚生労働省は12月20日の中医協総会(会長:小塩隆士・一橋大学経済研究所教授)に、2024年度薬価制度改革の骨子(案)を提案、承認された。日本の創薬力を強化するため、新薬創出・適応外薬解消等促進加算(新薬創出等加算)の要件や、市場拡大再算定の“共連れ”ルールを見直す。後発品については、安定供給を確保できる企業の品目を医療現場で選定しやすくなるよう、「後発品の安定供給が確保できる企業の評価指標及び評価方法」を導入して可視化、薬価制度でも活用する。改定の度に議論になる「調整幅」(薬価は市場実勢価格に調整幅を上乗せして決定)は2%のまま据え置く(資料は、厚労省のホームページ )。


1.2024(令和6)年度薬価制度改革における改革事項
補正加算の見直しは、2024(令和6)年度薬価制度改革における、「ドラッグ・ラグ/ドラッグ・ロス解消に向けた革新的な医薬品のイノベーション評価」に該当します。
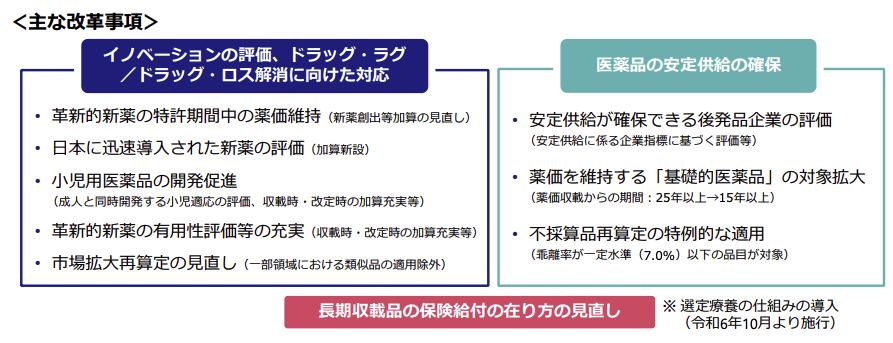
引用:中央社会保険医療協議会 総会(第574回)議事次第
2024(令和6)度薬価改定で実施された、「ドラッグ・ラグ/ドラッグ・ロス解消に向けた革新的な医薬品のイノベーション評価」に関する制度改革のうち、今回の記事で注目するものを赤字にしてみます。
ドラッグ・ラグ/ドラッグ・ロス解消に向けた革新的な医薬品のイノベーション評価の注目点
①日本への早期導入を促進するための評価
・迅速導入加算の新設
・薬価収載後の外国平均価格調整の見直し
②新薬創出・適応外薬解消等促進加算の見直し
・企業指標に基づく加算係数の設定(加算額の調整)廃止
・対象品目の追加(迅速導入品、小児用医薬品)
③新薬の薬価収載時の評価の見直し
・有用性系加算の定量的評価の評価項目の見直し
・補正加算における加算率付与の考え方の見直し
④新薬の薬価改定時における評価の見直し
・薬価改定時の加算の併算定
・薬価改定時の加算と新薬創出等加算の適用方法
⑤小児用医薬品の評価の見直し
・小児用医薬品の評価充実
・成人と小児の同時開発に係る評価
⑥市場拡大再算定の見直し
・類似品としての適用を除外する範囲の設定


2.迅速導入加算の新設
薬価収載時の評価(補正加算)に新たに迅速導入加算が加わります。
迅速導入加算
- 画期性加算:70〜120%
- 有用性加算(Ⅰ):35〜60%
- 有用性加算(Ⅱ):5〜30%
- 市場性加算(Ⅰ):10〜20%
- 市場性加算(Ⅱ):5%
- 特定用途加算:5〜20%
- 小児加算:5〜20%
- 先駆加算:10〜20%
- 迅速導入加算:5〜10%(令和6年度薬価制度改革で追加)
迅速導入加算は、その名前からイメージできるように、「革新的新薬を日本へ迅速に導入した場合の評価」です。具体的には以下の要件を全て満たすものが対象となります。
迅速導入加算の要件
- 国際共同試験(日本において臨床試験が実施されている場合に限る。)により開発された品目
(又は日本以外の国と同時若しくは日本以外の国より先に臨床試験を実施して開発された品目) - 医薬品医療機器等法第14条第10項の規定に基づき優先審査の対象となった品目
- その効能又は効果に関し、承認申請がアメリカ合衆国及び欧州(以下「欧米」という。)より早い
(又は欧米において最も早い承認申請から6ヶ月以内の品目) - その効能又は効果に関し、承認が欧米より早い又は欧米で最も早い承認から6ヶ月以内の品目
迅速導入加算と類似した加算に、先駆加算(旧 先駆け審査指定制度加算、旧々 先駆導入加算)がありますが、先駆加算は、世界に先駆けて日本での実用化された医薬品を評価であり、迅速導入加算は、それに準じた評価となります。

引用:中央社会保険医療協議会 総会(第574回)議事次第
迅速導入加算が登場したことで、先駆的医薬品の対象にならない医薬品も評価の対象となり、海外で開発されている画期的な医薬品がこれまでより早く国内に導入されることが期待されます。




































